Wpływ szoku termicznego na Pseudomonas fluorescens - praca badawcza z Olimpiady Biologicznej

Poniżej prezentuję pracę nominowaną do wyróżnienia na etapie centralnym Olimpiady Biologicznej w roku 2014/2015. Została ona oceniona na 46 pkt. Autor wykazał się zaangażowaniem poszukując wsparcia Warszawskiej placówki naukowej. Badania były kontynuowane w kolejnym roku, czego efekty również opublikuję.
Zamieszczone na stronie prace służą tylko zapoznaniu się z ogólnym charakterem prac badawczych zgłaszanych na Olimpiadę Biologiczną. Niedopuszczalne jest kopiowanie całej koncepcji wykonania pracy bądź fragmentów jej tekstu we własnej pracy. Tego typu działania będą uznawane za plagiat i mogą wiązać się z odrzuceniem pracy przez komisję olimpiady.
Wpływ szoku termicznego na odpowiedź na stres osmotyczny u Pseudomonas fluorescens
AUTOR: Maciej Piejko
Streszczenie
Celem niniejszego eksperymentu było doświadczalne sprawdzenie czy dla bakterii P. fluorescens zachodzi zjawisko synergii stresów termicznego i osmotycznego. Dwie hodowle bakteryjne były preinkubowane w warunkach temperatury optymalnej i stresowej, po czym zostały podzielone i umieszczone warunkach o różnym stopniu osmolarności. W warukach stresu osmotycznego zaobserwowano niewielki spadek śmiertelności komórek preinkubowanych w warunkach szoku termicznego.
Wstęp
Jednym z zagadnień mających duże znaczenie w wielu dziedzinach biologii jest odpowiedź komórek na stres środowiskowy wywołany różnymi czynnikami chemiczno-fizycznymi, m.in. niekorzystną temperaturą, ciśnieniem osmotycznym lub obecnością szkodliwych substancji w otoczeniu1. Dzięki badaniom w tym zakresie wiadomo, jakie możliwości adaptacyjne ma wybrany organizm, jaka jest jego podatność na określone zmiany środowiska. Komórka wystawiona na ich negatywny wpływ w miarę swych możliwości adaptuje się do nowych warunków, wykształcając najróżniejsze mechanizmy ochronne, by przetrwać. Najznaczniejsze zmiany obserwowane są na poziomie molekularnym i obejmują od zachodzenia prostych reakcji chemicznych, które pośrednio lub bezpośrednio zwiększają szanse komórki na przeżycie, aż do zmiany ekspresji genów, a czasem efektów widocznych dla oka ludzkiego2.
W warunkach naturalnych komórki mogą być narażone na działanie więcej niż jednego czynnika stresowego na raz. Reakcja na stres środowiskowy w zależności od jego charakteru oraz gatunku mikroorganizmu może być różna. Jeśli na komórkę zadziała jakikolwiek czynnik stresowy, to w miarę jej możliwości i nasilenia czynnika w komórce mogą zajść różnorakie zmiany, takie jak zmiana składu chemicznego cytoplazmy, parametrów fizycznych błon czy synteza białek hsp1. Te zmiany mogą sprawić, że komórka inaczej będzie znosiła inne rodzaje stresu. Zakładając, że mechanizm ochrony przed jednym czynnikiem stresowym jest w części podobny, powiązany ze sposobem ochrony przed innym, to prekondycjonowanie komórki odpowiednim stresorem mogłoby wyzwolić pewną reakcję odpornościową na inne stresory, lecz prawdziwe skutki takiego działania muszą być dokładniej poznane, by móc bardziej jednoznacznie określić tę zależność23. Taka synergia jest korzystna dla komórek, jeśli odpowiedzi na stres są skorelowane dodatnio. Efekt ten jest bardzo ogólny w działaniu, toteż prawdopodobne jest, że mógłby mieć szerokie zastosowanie praktyczne.
Materiały i metody
| Domena | Prokarionty |
| Królestwo | Bakterie |
| Typ | Proteobakterie |
| Klasa | Gammaproteobakterie |
| Rząd | Pseudomonadales |
| Rodzina | Pseudomonadaceae |
| Rodzaj | Pseudomonas |
| Gatunek | Pseudomonas fluorescens |
Tab. 1 Systematyka wykorzystanego gatunku [1]
Pseudomonas fluorescens jest bakterią spotykaną w glebie, wodzie, ściekach, powietrzu oraz powierzchni niektórych roślin. Nie stanowi poważnego zagrożenia dla człowieka i zwierząt, lecz zachowuje się jak patogen oportunistyczny i w odpowiednich warunkach może stać się przyczyną infekcji42. Odnotowano przypadki zakażeń krwi transfuzyjnej, które często niewykryte mogą prowadzić do śmierci pacjenta2. Jej nazwa gatunkowa pochodzi od syntetyzowanego przez nią barwnika, który emituje światło o barwie niebieskiej pod wpływem promieniowania UV4. Optymalny zakres temperatury dla jej rozwoju to 25-30°C4. W niedokładnie poznany sposób zapobiegają także infekcjom grzybicznym korzeni niektórych roślin poprzez stwarzanie niedoboru żelaza w ryzosferze oraz wydzielanie utylizowanych przez rośliny sideroforów23.
Badane mikroorganizmy pochodziły z kolekcji Instytutu Mikrobiologii Uniwersytetu Warszawskiego. Nie określono wykorzystanego szczepu bakterii. W celu wyznaczenia odpowiednich parametrów użytych w badaniu, tj. temperatury stresowej oraz stężeń molowych chlorku sodu wykonano kilka doświadczeń wstępnych. Następnie wybrano względnie najodpowiedniejsze z kilku wartości. Postąpiono tak, gdyż dla wybranej bakterii nie są dostępne wszystkie potrzebne do przeprowadzenia eksperymentu dane. Wszelkie działania umożliwione były dzięki życzliwości pracowników Instytutu Mikrobiologii UW, dzięki którym zyskano dostęp do laboratorium wraz z jego wyposażeniem.
Eksperyment prowadzono w dniach 1-2 września. Rozpoczął się od założenia hodowli nocnej w bulionie odżywczym o objętości 10ml, inkubowanej i wytrząsanej (przy prędkości 120 RPM) w temp. 30°C. Źródłem komórek był posiew redukcyjny wykonany w dniu 26.06.2014r. przechowywany w lodówce laboratoryjnej. Następnego dnia hodowlę rozcieńczono 20-krotnie w bulionie odżywczym (produkt Biocorp) i umieszczono w kolbie stożkowej o objętości 300ml. Kolbę umieszczono w wytrząsarce na czas 1h w temp. 30°C przy prędkości 120 RPM w celu wstępnej adaptacji i wejścia w fazę wzrostu wykładniczego komórek bakteryjnych.
Celem wyindukowania stresu termicznego u częsci bakterii hodowlę rozdzielono do dwóch identycznych kolb stożkowych o V=120ml. Jedną inkubowano wytrzasając w temp. 30°C, drugą w temp. 37°C przez 3h. W obu shakerach prędkość wytrząsania wynosiła 120 RPM. Co 1h pobierano po 1ml hodowli z każdej kolby do oddzielnych kuwet, aby wykonać pomiary absorbancji (OD). Wykonywano je spektrofotometrem Pharmacia Biotech Novaspec II (λ=600nm) w odniesieniu do czystej pożywki (bulion odżywczy). Po 3h zebrano także próbki przeznaczone do wysiewów. Wysiano rozcieńczenia 10-5 i 10-6 wszystkich próbek, każde w trzech powtórzeniach na agarze firmy Biocorp. Hodowle z obu kolb natychmiast po pobraniu próbek do analizy rozdzielono do 6 jednakowych kolb stożkowych (V=100ml) zawierających 3 stężenia NaCl: 0M, 1/2M i 1M.
Pomiary OD600 wykonywano co 1h przez cały czas trwania doświadczenia, a wysiewy wykonano po 3h inkubacji. Wysiano rozcieńczenia 10-4, 10-5, 10-6 bądź 10-7 (3 różne w zależności od dodanego stęż. chlorku sodu1). Spośród powyższych trzech do liczenia jtk/ml (jednostek tworzących kolonie/ml) wybrano optymalne rozcieńczenie. Wszystkie wysiewy wykonywano w trzech powtórzeniach. Z wyników pomiarów wyliczono średnią wartość wyników z każdego powtórzenia oraz odchylenie standardowe próbek. Następnie za pomocą programu Microsoft Excel 2010 stworzono tabele i wykresy zamieszczone w pracy.
1. Wybrane na podstawie doświadczeń wstępnych, które wykazały słuszność wykorzystania wybranych rozcieńczeń.
Wyniki
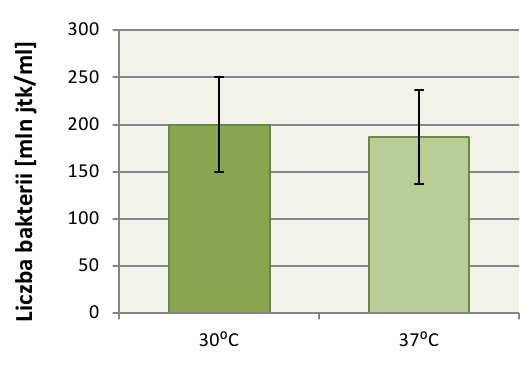
Dwie hodowle po 3-godzinnym okresie inkubacji w temperaturze optymalnej (30°C) i niekorzystnie wysokiej (37°C) wykazywały nieznaczną, lecz przewidywaną, odmienną żywotność (wyk.1). Hodowla umieszczona w temperaturze szoku termicznego zawierała mniej komórek zdolnych do tworzenia kolonii w porównaniu do hodowli rosnącej w warunkach korzystnych.
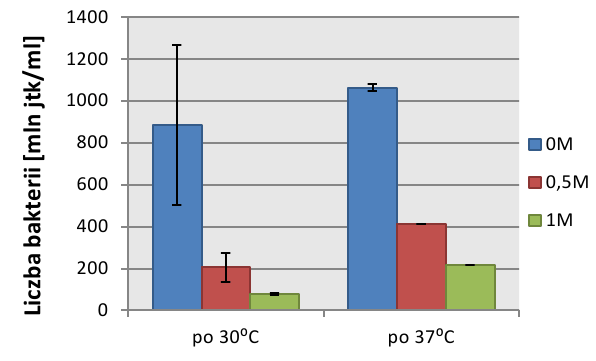
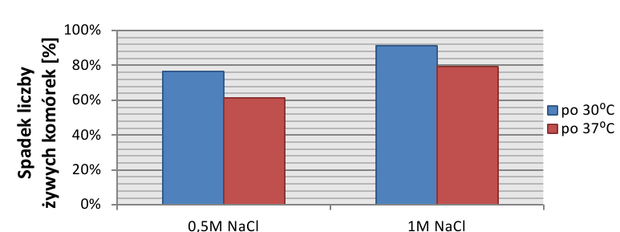
Po inkubacji rozdzielonych hodowli w temp. 30°C w różnych stęż. NaCl kondycja wszystkich z nich uległa znacznym zmianom. Hodowla umieszczona w warunkach optymalnych temperatury (30°C) i ciśnienia osmotycznego (0M NaCl2) wykazywała mniejszą żywotność – mniejszą liczbę komórek zdolnych do podziałów w stosunku do hodowli poddanej wcześniej 3-godzinnemu stresowi cieplnemu. Inne hodowle także wykazywały podobny trend – hodowle w odpowiadających sobie stężeniach rosły gorzej, jeśli wcześniej nie wystąpił stres termiczny. Z wykresu nr 2 wynika, że jeżeli hodowla inkubowana była wcześniej w temp. 37°C to komórki w niej zawarte lepiej znoszą zwiększoną osmolarność otoczenia (są bardziej odporne na jego działanie). Komórki poddane działaniu temperatury szoku termicznego wykazywały większą żywotność (niezależnie od stężenia dodanej soli) w stosunku do komórek, które nie miały kontaktu z wysoką temperaturą.
2. Pomijając zawartość NaC (=60mM/l)l i ciśnienie osmotyczne bulionu odżywczego, który jest roztworem izotonicznym względem komórek bakteryjnych
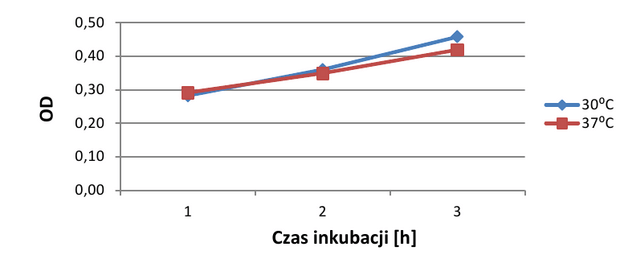
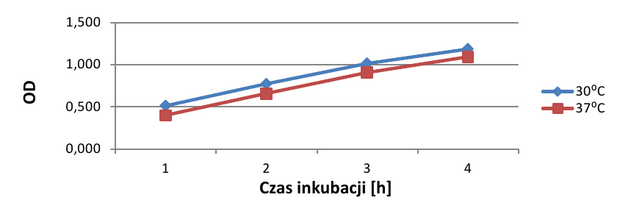
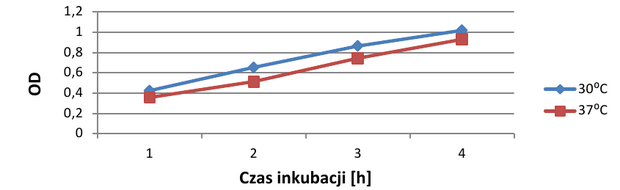
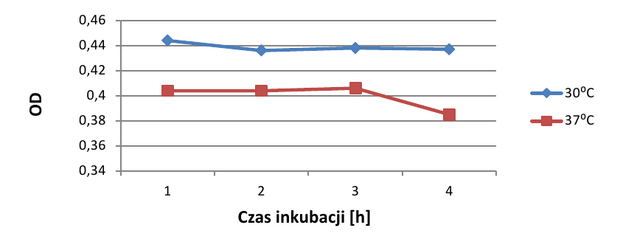
Odczyty pomiarów absorbancji zdają się rzucać inne światło na wyniki badania. W czasie pierwszych trzech godzin trwania doświadczenia gęstość optyczna obu hodowli rosła, lecz jej wartość między nimi różniła się bardzo nieznacznie. W niewielkim stopniu przewagę liczebną zaczęła zyskiwać hodowla inkubowana w temperaturze 30°C, co potwierdza fakt, że temperatura 37°C wpływa niekorzystnie na tę bakterię. W drugiej części eksperymentu (3-7h) tendencja pozostała podobna. W stężeniach 0M i 0,5M NaCl liczba komórek rosła w obu hodowlach, lecz gorzej, jeśli hodowla była inkubowana w temperaturze szoku cieplnego. W przypadku hodowli zawierającej 1M NaCl absorbancja utrzymywała się na podobnym poziomie i dopiero po szóstej godzinie trwania doświadczenia można powiedzieć o lekkim załamaniu w hodowli, która wcześniej doznała szoku termicznego.
Dyskusja
Pomiary gęstości optycznej informują jedynie o liczbie wszystkich komórek w roztworze, lecz na ich podstawie nie da się określić, ile z nich jest żywych, zdolnych do wytworzenia kolonii, czyli tak na prawdę to, co jest kluczowe. Z pomiarów OD wynika, że liczba komórek wzrastała (lub ulegała niewielkim zmianom), co przeczy wynikom uzyskanym z posiewów. Wynika z tego, że w roztworach przybywało komórek, lecz część z nich musiała obumrzeć dając fałszywy wynik. Z doświadczeń wstępnych wiadomo także, że komórki te po dłuższej ekspozycji na stres zarówno termiczny jak osmotyczny ulegają lizie (widoczne gołym okiem kłaczki w roztworze z jednoczesnym spadkiem absorbancji po ich sedymentacji).
Wpływ obecności stężenia 0,5M chlorku sodu w hodowli obniża kondycję bakterii. Z kolei stężenie 1M ma na nią bardzo negatywny wpływ (ocenianą na podstawie szybkości podziałów komórkowych). Oznacza to, że reakcja komórek na stres osmotyczny ma charakter wykładniczy, a odpowiedź na ten stresor zmienia się w zależności od nasilenia czynnika.
Odpowiednia temperatura jest niezbędna do istnienia wszystkich procesów metabolicznych w komórkach. Jej zbyt niska bądź wysoka wartość ma mniej lub bardziej negatywny wpływ na komórkę, jako że jest jednym z najbardziej podstawowych czynników zapewniających istnienie życia. Maksymalna temperatura z optymalnego zakresu do wzrostu, podziału komórek P. fluorescens wynosi 30°C4. Temperatury wyższe są dla niej zbyt wysokie i powodują adaptacyjne zmiany w komórkach. Bakteria ta przestaje rosnąć w 41°C i ginie w temp. 43°C, więc jest mezofilem4. W doświadczeniu wykazano, że wcześniejsze wystawienie komórek P. fluorescens na działanie wysokiej temperatury sprawia, że są bardziej odporne na gwałtowne zwiększenie się osmolarności otoczenia. Także ciśnienie osmotyczne środowiska jest ważnym elementem, który może łatwo ulegać gwałtownym zmianom, jednocześnie stwarzając niekorzystne warunki dla bakterii. Oba wybrane do badania stresory są jednymi z najbardziej podstawowych i często występujących stresorów abiotycznych, co uzasadnia pierwszorzędność dogłębnego zbadania ich wpływu na kondycję komórek.
Główną przyczyną zakażeń krwi transfuzyjnej przez P. fluorescens jest jej powszechna obecność w środowisku zewnętrznym np. na skórze2. Ponieważ filtracja krwi nie pomaga w jej oczyszczeniu trzeba zapobiegać temu zjawisku w inny sposób, a najłatwiejszym z nich jest z pewnością czyszczenie skóry przed pobraniem próbki krwi2. Z powodu występowania takich zdarzeń warto wiedzieć jak najwięcej na temat tej bakterii, by móc skuteczniej z nią walczyć. Dane na temat przeżywalności bakterii w najróżniejszych warunkach środowiska oraz jego zmienności mogą dać ogląd na to, jakie metody skuteczniej ją zwalczają lub promują wzrost.
Prekondycjonowanie bakterii może (jak wykazano w eksperymencie), lecz nie musi mieć pozytywne skutki dla niej. W zależności od rodzaju stresora reakcja komórek może byc dodatnia lub może nie zachodzić w ogóle (ogólne zjawisko zachodzące u drożdży jest podobne u bakterii)1. Wiedza o reakcjach komórek na stresy środowiskowe najbardziej przydaje się w wykorzystaniu biotechnologicznym, gdzie warunki wewnątrz bioreaktorów muszą być odpowiednio dostosowane do potrzeb, by móc polepszyć wydajność produkcji w bioreaktorach. Komórki P. fluorescens rezydujące w glebie mają zdolność do fitoprotekcyjnego działania na rośliny, przy których korzeniach bytują poprzez skuteczniejsze wychwytywanie żelaza z gleby niż mikroorganizmy atakujące korzenie tych roślin2. Dzięki temu rośliny mają większe szanse na przeżycie. Odbywa się pośrednio poprzez syntezę sideroforu – piowerdyny przez komórki bakterii, który jednocześnie odpowiada za jej fluorescensyjne cechy42. Wiedzę uzyskaną w tym i podobnych doświadczeniach można więc wykorzystać praktycznie na wiele sposobów.
Wszystkie wymienione przyczyny uzasadniają potrzebę dalszych badań nad bakterią Pseudomonas fluorescens, która przyczynia się do istnienia procesów zarówno szkodliwych dla człowieka, jak i takich, które umiejętnie wykorzystane mają rzeczywisty potencjał mu pomóc.
Literatura
-
Grajek W., Szymanowska D. (2008) Stresy środowiskowe działające na drożdże Saccharomyces cerevisiae w procesie fermentacji etanolowej ↩︎ ↩︎ ↩︎
-
Martins dos Santos V. A. P., Moore E. R. B., Palleroni N. J., Pieper D. H., Ramos J. L., Tindall B. J. Nonmedical: Pseudomonas W: Dworkin M., Falkow S., Rosenberg E., Schleifer K. H., Stackebrandt E. (2006) The Prokaryotes, A Handbook on the Biology of Bacteria: Proteobacteria: Gamma Subclass. Springer, vol. 6, 3rd edition ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎
-
Eberl L., van Elsas J. D., Givskov M., Molin S., van Overbeek L. S. (1995) Survival of, and Induced Stress Resistance in, Carbon-Starved Pseudomonas fluorescens Cells Residing in Soil ↩︎ ↩︎
-
Palleroni N. J., (2005) Pseudomonas W: Brenner D. J., Krieg N. R., Staley J. T. (red.) Bergey’s Manual of Systematic Bacteriology: The Proteobacteria, Part B The Gammaproteobacteria. Springer, vol. 2, 2nd edition. ↩︎ ↩︎ ↩︎ ↩︎ ↩︎ ↩︎
- Zaloguj się albo zarejestruj aby dodać komentarz
