Chemia - Informator CKE, Poziom rozszerzony (Formuła 2023) - Zadanie 37.
W analizie potencjometrycznej wykorzystuje się zależność potencjału odpowiednich elektrod od stężenia jonów oznaczanych. Pomiary potencjometryczne polegają na mierzeniu SEM ogniwa zestawionego z dwóch półogniw: tzw. elektrody wskaźnikowej, zanurzonej w badanym roztworze, oraz tzw. elektrody odniesienia, zanurzonej w roztworze o niezmiennym składzie, której potencjał w warunkach pomiaru pozostaje stały.
Rozróżnia się dwa główne typy elektrod. Elektrody pierwszego rodzaju to elektrody odwracalne względem kationu: są zbudowane z metalu i są w równowadze z roztworem zawierającym jony tego metalu (M oznacza symbol metalu):
M(s) + ⇄ Mn+(aq) + 𝑛e–
Elektrody drugiego rodzaju są odwracalne względem anionu, tworzącego z metalem elektrody trudno rozpuszczalny związek. Elektrodą drugiego rodzaju jest elektroda halogenosrebrowa. Działanie tej elektrody opisuje równanie (X oznacza symbol halogenu):
AgX(s) + e– ⇄ Ag(s) + X–(aq)
Przykładem elektrody halogenosrebrowej jest elektroda chlorosrebrowa:
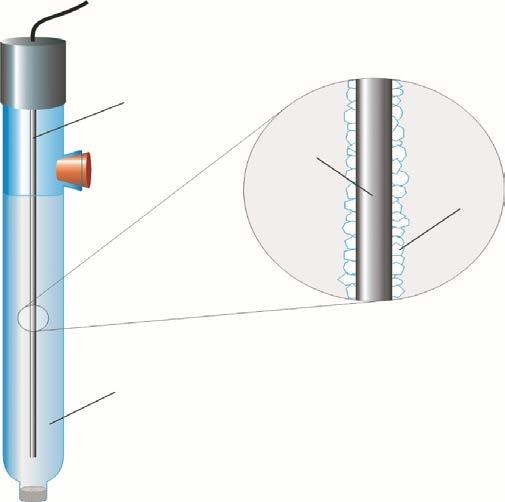
Działanie elektrody chlorosrebrowej opisuje równanie:
AgCl(s) + e− ⇄ Ag(s) + Cl− (aq)
Potencjał tej elektrody zależy od stężenia jonów chlorkowych w roztworze, który stanowi jej
element, i wyraża się równaniem: EAg/AgCl = EoAg/AgCl − 0,059log cCl− (w temperaturze 298 K).
Przygotowano dwie elektrody chlorosrebrowe: elektroda I zawierała wodny roztwór chlorku
potasu o stężeniu równym 0,10 mol ∙ dm–3, a elektroda II – wodny roztwór tej samej soli
o stężeniu równym 0,01 mol ∙ dm–3
Rozstrzygnij, która elektroda chlorosrebrowa (I czy II) ma – w tej samej temperaturze – wyższy potencjał. Odpowiedź uzasadnij.
Rozstrzygnięcie:
Uzasadnienie:
Rozwiązanie
Zasady oceniania
1 pkt – poprawne rozstrzygnięcie, w którym roztworze KCl (I czy II) potencjał elektrody
chlorosrebrowej w nim zanurzonej będzie wyższy, i poprawne uzasadnienie.
0 pkt – odpowiedź niespełniająca powyższego kryterium albo brak odpowiedzi.
Przykładowe rozwiązania
Rozstrzygnięcie: II.
Uzasadnienie:
Potencjał elektrody chlorosrebrowej zależy od stężenia jonów chlorkowych w roztworze,
zgodnie z równaniem: EAg/AgCl = EoAg/AgCl − 0,059log cCl− (w temperaturze 298 K). Wartość log cCl− jest tym większa, im większe jest stężenie jonów chlorkowych, więc im większe
stężenie jonów chlorkowych, tym niższa wartość potencjału elektrody.
ALBO
W roztworze I cCl− = 0,10 mol ∙ dm−3, więc
EAg/AgCl = EoAg/AgCl − 0,059log cCl− = EoAg/AgCl − 0,059log 10−1 = EoAg/AgCl + 0,059
W roztworze II cCl− = 0,01 mol ∙ dm−3, więc EAg/AgCl = EoAg/AgCl − 0,059log cCl− = EoAg/AgCl − 0,059log 10−2 = EoAg/AgCl + 0,118
⇒ EoAg/AgCl + 0,118 > EoAg/AgCl + 0,059
