Chemia - Zbiór zadań problemowych CKE, Poziom rozszerzony (Formuła 2023) - Zadanie 6.
Cząsteczki kwasu etanowego mogą łączyć się wiązaniami wodorowymi i tworzyć dimer:
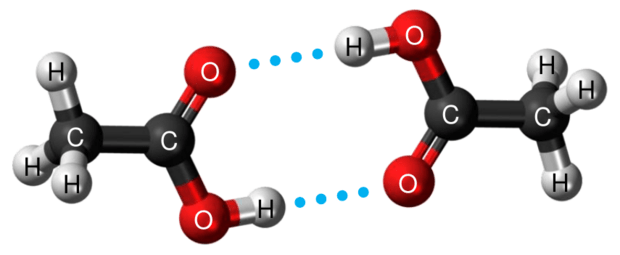
Ten dimer występuje w stanie gazowym oraz w roztworach kwasu etanowego w rozpuszczalnikach nietworzących z nim wiązań wodorowych.
Roztwór 60,0 g kwasu octowego (1,00 mol) w 100,0 g benzenu wykazuje temperaturę wrzenia wyższą o 20,1°C względem wrzenia czystego benzenu. Podwyższenie temperatury wrzenia rozpuszczalnika jest proporcjonalne do łącznej liczby drobin substancji rozpuszczonej w rozpuszczalniku. Tę zależność opisuje poniższy wzór:
Δ𝑡 = 𝐾b ∙ 𝑛𝑚r
gdzie Δ𝑡 to różnica temperatury wrzenia roztworu i czystego rozpuszczalnika (wyrażona w °C), 𝑛 – sumaryczna liczba drobin w roztworze (wyrażona w molach), 𝑚r – masa rozpuszczalnika (wyrażona w kilogramach), a 𝐾b – stała ebulioskopowa, której wartość dla benzenu wynosi 2,51°C ∙ kg ∙ mol–1.
Oblicz stężeniową stałą równowagi reakcji:
2CH3COOH ⇄ (CH3COOH)2
w temperaturze T. W obliczeniach pomiń autodysocjację kwasu octowego i przyjmij, że otrzymany roztwór CH3COOH w benzenie miał gęstość równą 0,96 g ∙ cm–3.
Rozwiązanie
Zasady oceniania
4 pkt – rozwiązanie zawierające poprawnie zastosowaną metodę prowadzącą do poprawnego obliczenia wartości stałej równowagi reakcji dimeryzacji.
3 pkt – wyznaczenie liczby cząsteczek kwasu octowego oraz cząsteczek dimeru w stanie równowagi w roztworze, wyznaczenie (korzystając z podanego równania) sumarycznej liczby drobin w roztworze, poprawne obliczenie stężeń molowych kwasu octowego i jego dimeru w roztworze.
ALBO
– obliczenie wartości stałej równowagi reakcji, ale rozwiązanie zawiera błędy (arytmetyczne, wynik jest podany z błędną jednostką lub bez jednostki).
2 pkt – wyznaczenie liczby cząsteczek kwasu octowego oraz cząsteczek dimeru w stanie równowagi w roztworze, wyznaczenie (korzystając z podanego równania) sumarycznej liczby drobin w roztworze.
ALBO
– wyznaczenie liczby cząsteczek kwasu octowego oraz cząsteczek dimeru w stanie równowagi w roztworze, wyznaczenie (korzystając z podanego równania) sumarycznej liczby drobin w roztworze, obliczenie stężeń molowych kwasu octowego i jego dimeru w roztworze, ale rozwiązanie zawiera błędy (arytmetyczne, wynik jest podany z błędną jednostką lub bez jednostki).
1 pkt – wyznaczenie liczby cząsteczek kwasu octowego oraz cząsteczek dimeru w stanie równowagi w roztworze.
ALBO
– wyznaczenie liczby cząsteczek kwasu octowego oraz cząsteczek dimeru w stanie równowagi w roztworze, wyznaczenie (korzystając z podanego równania) sumarycznej liczby drobin w roztworze, ale rozwiązanie zawiera błędy (arytmetyczne, wynik jest podany z błędną jednostką lub bez jednostki).
0 pkt – rozwiązanie całkowicie błędne albo brak rozwiązania.
Przykładowe rozwiązanie
Przekształcając równanie podane w treści zadania, otrzymujemy wzór pozwalający obliczyć sumaryczną liczbę drobin (wyrażoną w molach) kwasu octowego w roztworze benzenowym:
𝑛 = Δ𝑡 ∙ 𝑚r𝐾b = 20,1°C ∙ 0,1000 kg2,51 °C ∙ kgmol = 0,801 mol
Widzimy więc, że chociaż do roztworu wprowadzono 1 mol cząsteczek kwasu octowego, to efektywna liczba cząsteczek w roztworze jest mniejsza, ze względu na tworzenie się dimerów cząsteczek kwasu octowego. Znając sumaryczną liczbę cząsteczek w roztworze, możemy obliczyć liczbę cząsteczek kwasu octowego oraz liczbę cząsteczek dimeru:
𝑛 = 1,00 – 2𝑥 + 𝑥 = 0,801, 𝑥 = 0,199 mol
𝑛kCH3COOH = 1,00 – 2𝑥 = 0,602 mol, 𝑛k(CH3COOH)2= 0,199 mol
Aby obliczyć stężenia równowagowe poszczególnych drobin, musimy znać objętość roztworu: 𝑚roztwór = 𝑚r + 𝑚kwas octowy = 100,0 g + 60,0 g = 160,0 g
𝑉= 𝑚roztwór𝑑 = 160,0 g0,96 gcm3 = 167 cm3 = 0,167 dm3
[CH3COOH] = 1,00 – 2𝑥𝑉 = 0,602 mol0,167 dm3 = 3,60 moldm3
[(CH3COOH)2] = 𝑥𝑉 = 0,199 mol0,167 dm3 = 1,19 moldm3
𝐾= [(CH3COOH)2][CH3COOH]2 = 1,193,62 = 0,092
