Chemia - Arkusz pokazowy CKE Marzec 2022, Poziom rozszerzony (Formuła 2023) - Zadanie 11.
Sól Mohra to zwyczajowa nazwa siarczanu(VI) żelaza(II) i amonu o wzorze (NH4)2Fe(SO4)2. W laboratorium chemicznym ten związek jest często używany jako wygodne i stabilne źródło jonów żelaza(II). Zarówno sama sól Mohra, jak i jej wodne roztwory są odporne na utlenianie na powietrzu.
Przeprowadzono dwuetapowe doświadczenie. W pierwszym etapie do dwóch probówek (A i B) z roztworem soli Mohra dodano wodny roztwór wodorotlenku sodu. Wynik doświadczenia w obu probówkach był identyczny i został przedstawiony na fotografii. W czasie doświadczenia zaszła reakcja chemiczna opisana równaniem:
Zaobserwowano również, że zwilżony uniwersalny papierek wskaźnikowy umieszczony u wylotu probówki zabarwił się na niebiesko.
11.1. (0–1)
Napisz w formie jonowej skróconej równanie reakcji zachodzącej po dodaniu wodnego roztworu wodorotlenku sodu, w wyniku której powstała substancja odpowiedzialna za zmianę barwy uniwersalnego papierka wskaźnikowego.
11.2. (0–1)
W drugim etapie doświadczenia do zawartości probówki A otrzymanej w poprzednim etapie dodano wodę utlenioną, czyli roztwór nadtlenku wodoru o stężeniu 3 %. Wynik tej części doświadczenia przedstawiono na fotografii.
Napisz w formie cząsteczkowej równanie reakcji zachodzącej w probówce A.
11.3. (0–1)
Probówkę B pozostawiono przez dłuższy czas na powietrzu. W probówce zaobserwowano zmiany, które zilustrowano na poniższych fotografiach.
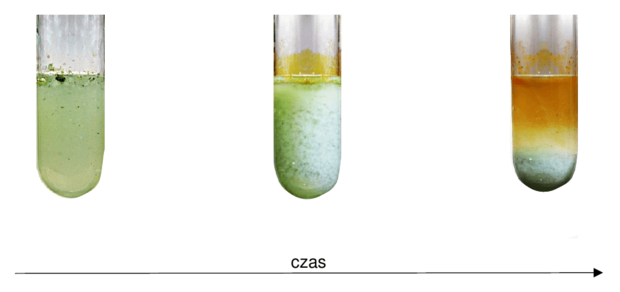
Wyjaśnij przyczyny obserwowanych zmian w probówce B pomimo niedodania do tej probówki żadnego odczynnika.
Wyjaśnienie:
Rozwiązanie
11.1. (0–1)
Zasady oceniania
1 pkt – poprawne napisanie równania reakcji.
0 pkt – odpowiedź niespełniająca powyższego kryterium albo brak odpowiedzi.
Rozwiązanie
NH+4 + OH– → NH3(↑) + H2O
11.2. (0–1)
Zasady oceniania
1 pkt – poprawne napisanie równania reakcji.
0 pkt – odpowiedź niespełniająca powyższego kryterium albo brak odpowiedzi.
Rozwiązanie
2Fe(OH)2 + H2O2 → 2Fe(OH)3
11.3. (0–1)
Zasady oceniania
1 pkt – poprawne wyjaśnienie odwołujące się do obecności w wodzie rozpuszczonego w niej tlenu, który pełni funkcję utleniacza.
0 pkt – odpowiedź niespełniająca powyższego kryterium albo brak odpowiedzi.
Przykładowe rozwiązania
W wodzie jest rozpuszczony tlen z powietrza, który w warunkach doświadczenia pełni funkcję utleniacza – w wyniku reakcji chemicznej (zielonkawy) Fe(OH)2 utlenia się do (pomarańczowego) Fe(OH)3.
ALBO
Zaszła reakcja chemiczna z rozpuszczonym w wodzie tlenem, który pełni funkcję utleniacza.


