Matura Maj 2025, Poziom rozszerzony (Formuła 2023) - Zadanie 6. (1 pkt)
Uczniowie wykonali dwuetapowe doświadczenie, którego celem było otrzymanie czystego tlenku miedzi(II). W pierwszym etapie strącili wodorotlenek miedzi(II), a w drugim etapie przeprowadzili jego rozkład termiczny w łaźni wodnej. Następnie uzyskaną mieszaninę przesączyli, żeby wyodrębnić stały produkt.
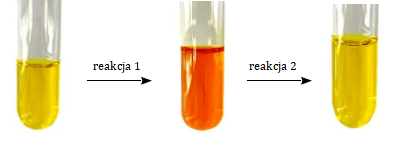
Na poniższym schemacie przedstawiono pierwszy etap doświadczenia.
Rozstrzygnij, w której probówce (I czy II) otrzymano osad tylko tlenku metalu. Odpowiedź uzasadnij.
Rozstrzygnięcie:
Uzasadnienie: