Chemia - Matura Czerwiec 2024, Poziom rozszerzony (Formuła 2015) - Zadanie 2.
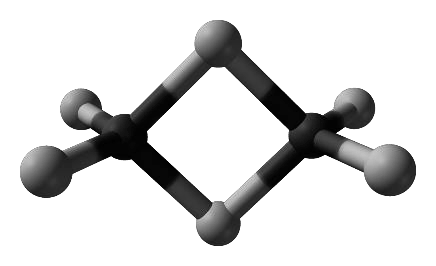
Gal tworzy trihalogenki, np. chlorek galu(III). W fazie stałej chlorek galu(III) występuje głównie w postaci dimerów, a w fazie gazowej – jako mieszanina dimerów i monomerów. Monomer chlorku galu(III) jest płaską cząsteczką, w której wszystkie atomy chloru są równocenne. Model dimeru przedstawiono na rysunku.
2.1. (0–1)
Narysuj wzór elektronowy monomeru chlorku galu(III). Zaznacz kreskami wiążące i wolne pary elektronowe.
Wzór monomeru chlorku galu(III):
2.2. (0–1)
Uzupełnij tabelę. Napisz, jaki typ hybrydyzacji (sp, sp2 albo sp3) przypisuje się orbitalom walencyjnym atomu galu w monomerze oraz w dimerze chlorku galu(III).
| Chlorek galu(III): | monomer | dimer |
|---|---|---|
| Typ hybrydyzacji |
2.3. (0–1)
Wyjaśnij, dlaczego monomery chlorku galu(III) mają zdolność łączenia się w dimery. Uwzględnij sposób powstawania wiązań, dzięki którym z monomeru chlorku galu(III) powstaje dimer.
Rozwiązanie
2.1. (0–1)
Zasady oceniania
1 pkt – poprawne narysowanie wzoru elektronowego (kreskowego lub kropkowego)
monomeru chlorku galu(III).
0 pkt – odpowiedź niespełniająca powyższego kryterium albo brak odpowiedzi.
Rozwiązanie
Uwaga: Geometria cząsteczki nie podlega ocenie.
2.2. (0–1)
Zasady oceniania
1 pkt – poprawne uzupełnienie tabeli – poprawne napisanie typu hybrydyzacji w monomerze
oraz w dimerze chlorku galu(III).
0 pkt – odpowiedź niespełniająca powyższego kryterium albo brak odpowiedzi.
Rozwiązanie
| Chlorek galu(III): | monomer | dimer |
|---|---|---|
| Typ hybrydyzacji | sp2 | sp3 |
2.3. (0–1)
Zasady oceniania
1 pkt – poprawne wyjaśnienie uwzględniające sposób powstawania wiązań, dzięki którym
z monomeru chlorku galu(III) powstaje dimer.
0 pkt – odpowiedź niespełniająca powyższego kryterium albo brak odpowiedzi.
Przykładowe rozwiązanie
W monomerze atom centralny (galu) nie osiągnął oktetu elektronowego, a atomy chloru mają
wolne pary elektronowe. Atom chloru jest donorem pary elektronowej wiązania z atomem
galu.
Uwaga: Do uzyskania pozytywnej oceny wyjaśnienie musi zawierać 3 elementy:
- informację o deficycie elektronowym atomu galu w monomerze
- informację o wolnych parach elektronowych atomów chloru
- sposób powstawania wiązania.
