Chemia - Zbiór zadań CKE, Poziom rozszerzony (Formuła 2015) - Zadanie 143.
Trzy gazowe związki organiczne: etyn, metan i metyloaminę wprowadzono do trzech zbiorników napełnionych gazowym chlorowodorem – każdy związek do innego zbiornika. Stwierdzono, że w dwóch zbiornikach zaszła reakcja chemiczna.
Wskaż związki organiczne, które w opisanym doświadczeniu wzięły udział w reakcji z chlorowodorem. Podaj ich nazwy i napisz wzory półstrukturalne (grupowe) związków, które powstały w reakcji z chlorowodorem tych związków organicznych.
Wskazówki
Aby poprawnie rozwiązać to zadanie, należy przeanalizować budowę cząsteczek użytych w doświadczeniu związków i wynikające z niej właściwości tych związków. Spośród nich tylko metan nie reaguje z chlorowodorem (pamiętamy, że jest to związek mało reaktywny).
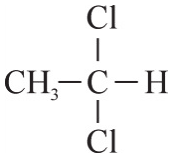
Pozostałe 2 związki – etyn i metyloamina – z chlorowodorem będą reagować. Etyn o wzorze CH≡CH jest węglowodorem nienasyconym, w jego cząsteczkach między atomami węgla występuje wiązanie potrójne, co uzdalnia etyn do udziału w reakcjach addycji. Po przyłączeniu 1 cząsteczki chlorowodoru do cząsteczki etynu powstanie związek nienasycony o wzorze CH2=CHCl, a po przyłączeniu kolejnej cząsteczki – związek nasycony o wzorze CH3–CHCl2 (pamiętamy o tym, że kolejny atom wodoru przyłącza się do atomu węgla „bogatszego w wodór”).
W przypadku metyloaminy zdolność do reagowania z chlorowodorem wynika z faktu, że atom azotu grupy aminowej –NH2 ma wolną parę elektronową i stanowi ujemny biegun cząsteczki, może więc oderwać proton od cząsteczki chlorowodoru. Powstają wówczas jony CH3–NH+3 i Cl–, tworzące związek jonowy o wzorze CH3–NH+3Cl–, czyli chlorowodorek metyloaminy.