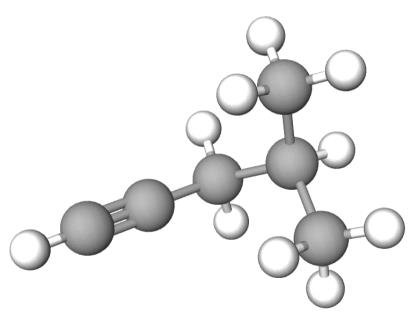
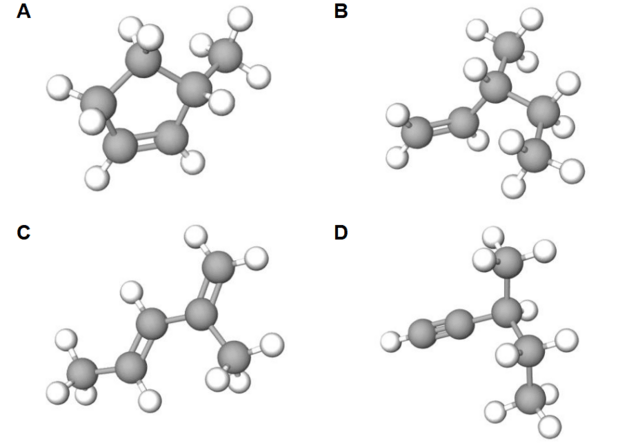
Matura Maj 2024, Poziom rozszerzony (Formuła 2023) - Zadanie 17. (2 pkt)
Cykloalkany ulegają analogicznym reakcjom jak alkany.
Benzen, cykloheksan i styren to węglowodory, które w temperaturze pokojowej są
bezbarwnymi cieczami. Ich wzory przedstawiono poniżej:
W trzech naczyniach znajdowały się oddzielnie i w przypadkowej kolejności: benzen, cykloheksan i styren. W celu identyfikacji tych substancji wykonano dwuetapowe doświadczenie. W pierwszym etapie do trzech probówek zawierających wodny roztwór manganianu(VII) potasu w środowisku obojętnym wprowadzono po jednej z badanych substancji. Następnie każdą probówkę zamknięto korkiem i wstrząśnięto. Po pewnym czasie zawartości probówek przybrały wygląd pokazany na zdjęciach.
W pierwszym etapie zidentyfikowano jeden z trzech węglowodorów. W drugim etapie doświadczenia do próbek niezidentyfikowanych węglowodorów wprowadzono stężony kwas azotowy(V) z dodatkiem stężonego kwasu siarkowego(VI) – i ogrzano zawartości probówek. Wyniki drugiego etapu doświadczenia przedstawiono na poniższych zdjęciach.
17.1. (0–1)
Napisz wzór sumaryczny związku manganu, który powstał w wyniku reakcji zachodzącej w pierwszym etapie doświadczenia, oraz wzór półstrukturalny (grupowy) lub uproszczony organicznego produktu tej przemiany.
| Wzór związku manganu | Wzór produktu organicznego |
|---|---|
17.2. (0–1)
Napisz równanie reakcji, która umożliwiła odróżnienie związków w drugim etapie doświadczenia.