Matura Czerwiec 2024, Poziom rozszerzony (Formuła 2015) - Zadanie 1. (3 pkt)
Dwa pierwiastki E i X tworzą jony E+ i X– o takiej samej konfiguracji elektronowej 1s22s22p63s23p6 (stan podstawowy). W atomie jednego z trwałych izotopów pierwiastka E liczba nukleonów jest o 20 większa od liczby protonów.
1.1. (0–1)
Uzupełnij poniższy schemat. Wpisz w odpowiednie pola symbol pierwiastka E, jego liczbę atomową oraz liczbę masową opisanego izotopu.
1.2. (0–1)
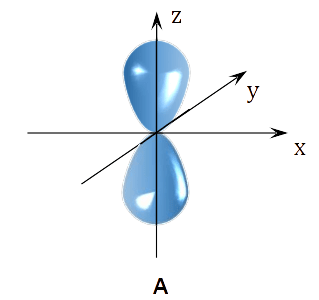
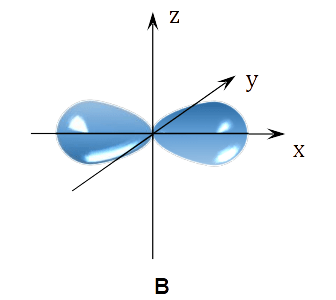
Napisz fragment konfiguracji elektronowej atomu X w stanie podstawowym opisujący rozmieszczenie elektronów walencyjnych na orbitalach. Zastosuj graficzny (klatkowy) zapis konfiguracji elektronowej. W zapisie uwzględnij numer powłoki i symbole podpowłok.
1.3. (0–1)
Pierwiastek E przyjmuje w związkach chemicznych jeden stopień utlenienia, a pierwiastek X tworzy związki, w których występuje na różnych stopniach utlenienia.
Określ charakter chemiczny (kwasowy, zasadowy, amfoteryczny, obojętny) tlenku pierwiastka E. Napisz wzór sumaryczny tlenku pierwiastka X, w którym ten pierwiastek przyjmuje najwyższy stopień utlenienia.
Charakter chemiczny tlenku pierwiastka E:
Wzór sumaryczny tlenku pierwiastka X na najwyższym stopniu utlenienia: