Matura Czerwiec 2021, Poziom rozszerzony (Formuła 2015) - Zadanie 8. (1 pkt)
Do reaktora, w którym znajdowała się stała substancja X, wprowadzono pod ciśnieniem atmosferycznym gazową substancję Y i zapoczątkowano reakcję chemiczną, w wyniku której powstawał gaz Z. Po 10 minutach, w temperaturze T1, ustaliła się równowaga opisana równaniem:
X (s) + Y (g) ⇄ Z (g)
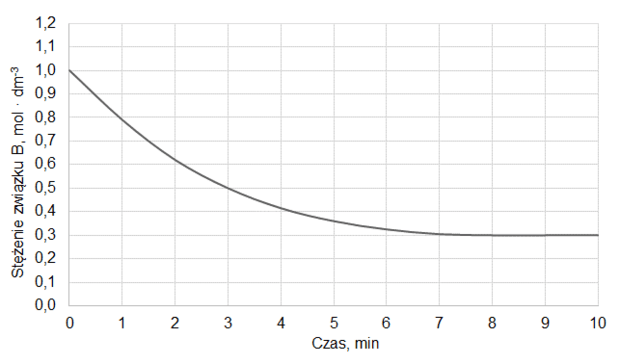
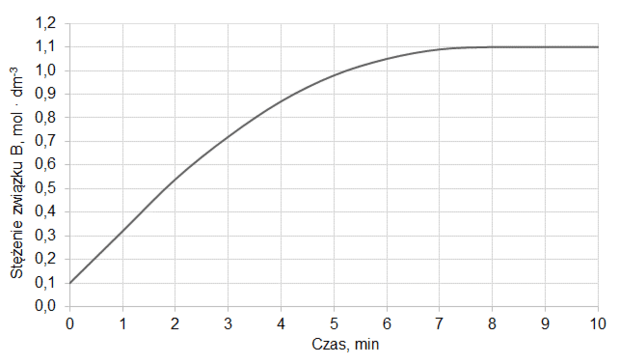
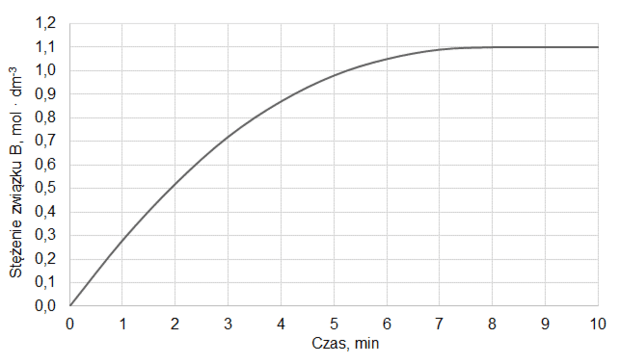
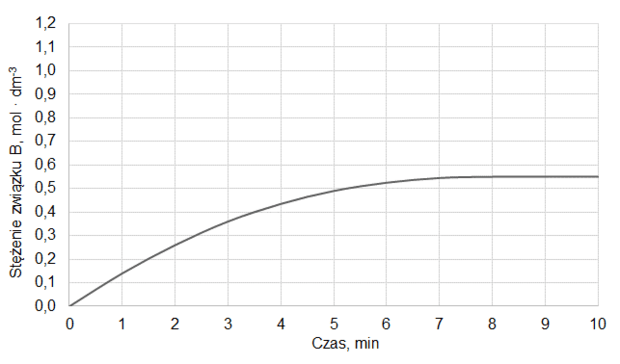
Na wykresie przedstawiono wyniki pomiaru liczby moli gazowych reagentów w trakcie trwania procesu oraz po ustaleniu się stanu równowagi w temperaturze T1. W piętnastej minucie eksperymentu zmieniono w układzie temperaturę na T2 wyższą od T1, czego konsekwencją było ustalenie się nowego stanu równowagi po dwudziestu minutach eksperymentu, co także zilustrowano na poniższym wykresie.
Napisz wyrażenie na stężeniową stałą równowagi reakcji tworzenia związku Z i oszacuj jej wartość w temperaturze T1. Uwzględnij fakt, że w wyrażeniu na stałą równowagi tej reakcji pomija się stężenie substancji stałej.
Wyrażenie na stałą równowagi:
Oszacowana wartość stałej równowagi: