Matura Czerwiec 2019, Poziom rozszerzony (Formuła 2015) - Zadanie 4. (2 pkt)
Stężeniowa stała równowagi reakcji
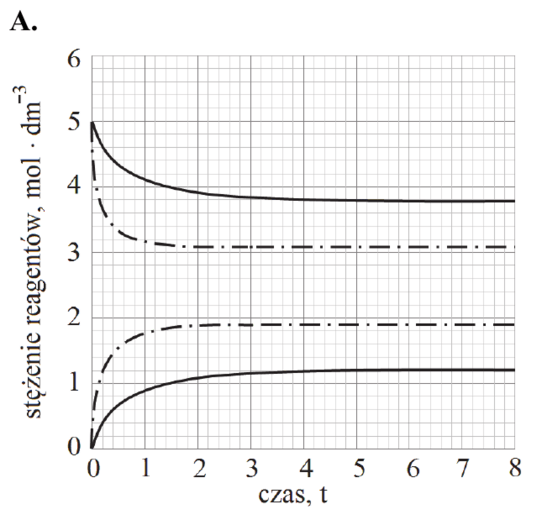
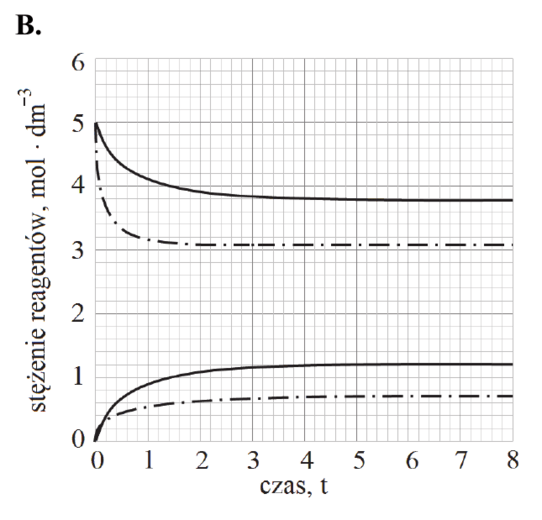
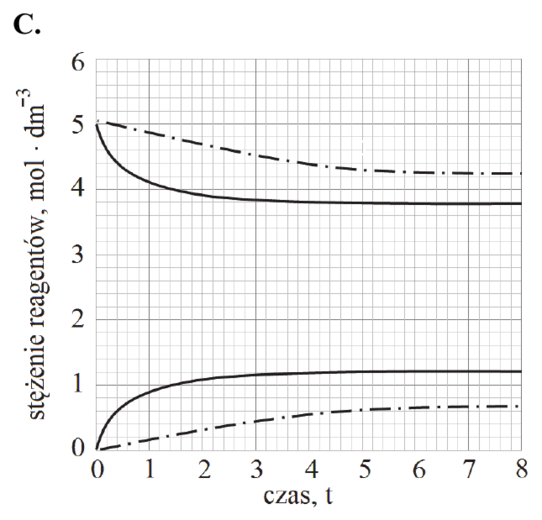
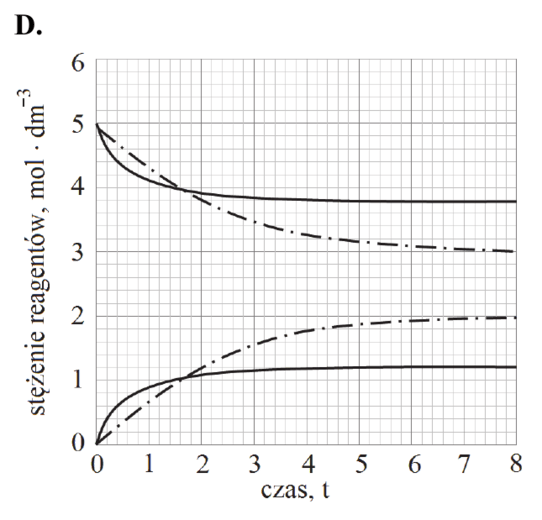
CO (g) + H2O (g) ⇄ CO2 (g) + H2 (g)
w temperaturze 1000 K jest równa 1.
Na podstawie: J. Sawicka, A. Janich-Kilian, W. Cejner-Mania, G. Urbańczyk, Tablice chemiczne, Gdańsk 2001.
W reaktorze o stałej pojemności znajdowało się 6 moli tlenku węgla(II).
Oblicz, ile moli wody (w postaci pary wodnej) należy wprowadzić do reaktora, aby po ustaleniu się równowagi w temperaturze 1000 K liczba moli wodoru była dwa razy większa od liczby moli tlenku węgla(II).