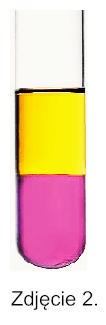Matura Maj 2025, Poziom rozszerzony (Formuła 2023) - Zadanie 9. (2 pkt)
Pod wyciągiem przeprowadzono dwa doświadczenia, których celem było zbadanie przebiegu reakcji metali z kwasami. Użyto poniższych odczynników:
Każdy z reagentów został użyty tylko raz. Przebieg doświadczeń przedstawiono na poniższych zdjęciach.

Napisz w formie jonowej skróconej równania reakcji zachodzących podczas doświadczeń 1. i 2.
Doświadczenie 1.:
Doświadczenie 2.: