Matura Maj 2025, Poziom rozszerzony (Formuła 2023) - Zadanie 5. (4 pkt)
W odpowiednich warunkach fluorowce mogą ze sobą reagować i tworzyć tzw. związki międzyhalogenowe o wzorze ogólnym AX𝑦, w którym 𝑦 przyjmuje wartość 1, 3, 5 lub 7. W tym wzorze A oznacza pierwiastek o mniejszej elektroujemności, a X – pierwiastek o większej elektroujemności.
Przykładem związku międzyhalogenowego jest trichlorek jodu o wzorze ICl3.
5.1. (0–2)
Trichlorek jodu został po raz pierwszy otrzymany w reakcji, której schemat przedstawiono poniżej.
IO–3 + I2 + H+ + Cl– → ICl3 + H2O
Napisz w formie jonowej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy), równanie reakcji redukcji zachodzącej podczas tej przemiany. Uwzględnij środowisko reakcji. Uzupełnij współczynniki stechiometryczne w poniższym schemacie.
Równanie reakcji redukcji:
IO–3 + I2 + H+ + Cl– → ICl3 + H2O
5.2. (0–2)
Metoda VSEPR pozwala określać kształt cząsteczek zbudowanych z atomów pierwiastków grup 1.–2. oraz 13.–18. W cząsteczce należy wyróżnić atom centralny (np. atom tlenu w cząsteczce H2O) i ustalić liczbę wolnych par elektronowych na jego zewnętrznej powłoce (𝑦). Następnie trzeba zsumować liczbę podstawników związanych z atomem centralnym (𝑥) i liczbę jego wolnych par elektronowych (𝑦). W ten sposób otrzymuje się tzw. liczbę przestrzenną (𝐿p = 𝑥 + 𝑦), która decyduje o kształcie cząsteczki. Ponieważ zarówno wolne, jak i wiążące pary elektronowe wzajemnie się odpychają, wszystkie elementy składające się na liczbę przestrzenną (podstawniki i wolne pary elektronowe) zajmują jak najbardziej odległe od siebie położenia wokół atomu centralnego.
oraz J.D. Lee, Zwięzła chemia nieorganiczna, Warszawa 1997.
Przedstawiony poniżej model jest ilustracją kształtu cząsteczki zbudowanej z atomu centralnego związanego z trzema podstawnikami (𝑥 = 3), dla 𝐿p = 4.
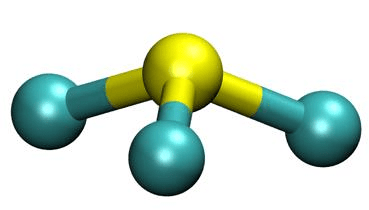
Narysuj wzór elektronowy cząsteczki trichlorku jodu ICl3. Zaznacz kreskami pary elektronowe wiązań chemicznych oraz wolne pary elektronowe. Następnie rozstrzygnij, czy przedstawiony model jest ilustracją kształtu cząsteczki ICl3. Napisz wartość liczby przestrzennej cząsteczki ICl3.
Rozstrzygnięcie:
Liczba przestrzenna ICl3 : 𝐿p =

