Arkusz pokazowy CKE Marzec 2022, Poziom rozszerzony (Formuła 2023) - Zadanie 28. (1 pkt)
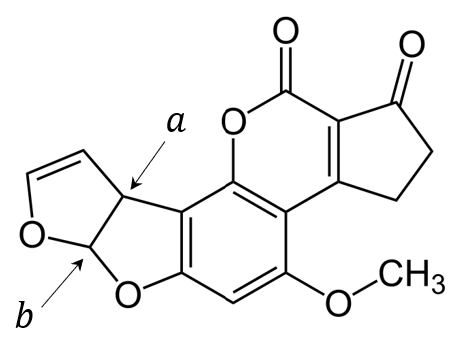
Poniżej przedstawiono wzór estru, w którego cząsteczkach są obecne dwa asymetryczne atomy węgla – oznaczone gwiazdką:
W laboratorium przeprowadzono reakcję, w której racemiczną mieszaninę kwasu 2-chloropropanowego (równomolową mieszaninę obu enancjomerów) poddano reakcji estryfikacji z jednym z enancjomerów 2-metylobutan-1-olu. W wyniku tej reakcji otrzymano dwa rodzaje estrów.
Napisz w formie jonowej skróconej równanie hydrolizy zasadowej estru opisanego w informacji. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.