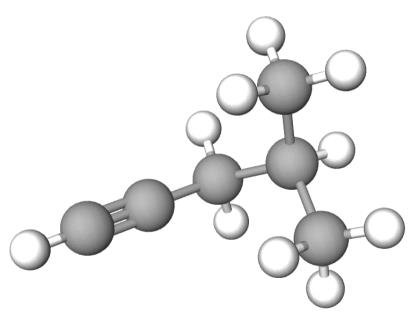
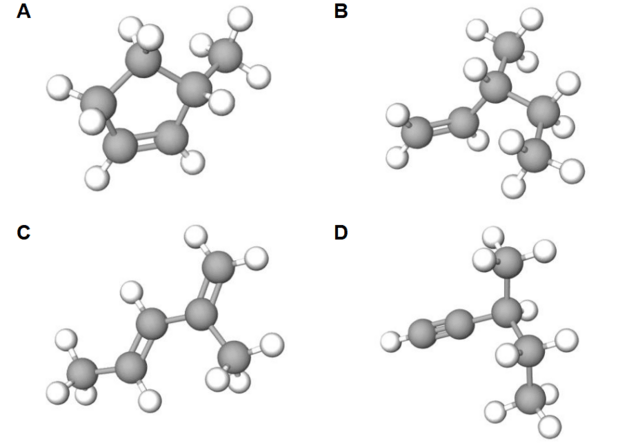
Zadania dodatkowe matury dwujęzycznej (tłumaczenie BiologHelp) Maj 2024, Poziom rozszerzony (Formuła 2023) - Zadanie 17. (2 pkt)
Poniżej przedstawiono ciąg przemian etanu i jego pochodnych:
C2H6 Cl2, światłoreakcja 1 C2H5Cl KOH (aq)reakcja 2 C2H5OH Al2O3, ogrzewaniereakcja 3 C2H4 Br2 (aq)reakcja 4 związek Y
17.1. (0–1)
Uzupełnij poniższą tabelę. Wpisz numery wszystkich reakcji kwalifikujących się do typu reakcji podanej w nagłówku każdej kolumny.
| Addycja | Eliminacja | Substytucja |
|---|---|---|
17.2. (0–1)
Uzupełnij poniższe zdanie. Wybierz i podkreśl poprawną odpowiedź spośród opcji podanych w nawiasie. Napisz wzór półstrukturalny (grupowy) związku Y.
Reakcja 1 zachodzi według mechanizmu (elektrofilowego / nukleofilowego / rodnikowego).
Wzór półstrukturalny (grupowy) związku Y: