Test diagnostyczny CKE Grudzień 2022, Poziom rozszerzony (Formuła 2023) - Zadanie 30. (1 pkt)
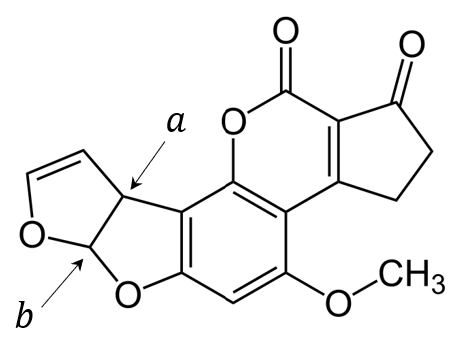
Wanilina jest popularną substancją zapachową stosowaną w przemyśle spożywczym i kosmetycznym. Strukturę cząsteczki tego związku przedstawia wzór I.
W jednej z metod otrzymywania waniliny produktem pośrednim jest związek opisany wzorem II.
Wśród wymienionych niżej odczynników wybierz te, które reagują z grupami funkcyjnymi oznaczonymi we wzorze waniliny cyframi (1) i (2). Wpisz te cyfry w odpowiednie komórki poniższej tabeli.
| Odczynnik | [Ag(NH3)2]OH (aq) | NaCl (aq) | KOH (aq) |
| Grupa funkcyjna |