Matura Maj 2025, Poziom rozszerzony (Formuła 2023) - Zadanie 12. (3 pkt)
Próbkę chlorku amonu o masie 0,10 g rozpuszczono w wodzie i otrzymano 100 cm3 roztworu. W powstałym roztworze kationy amonowe w pewnym stopniu ulegają przemianie zgodnie z poniższym równaniem.
NH+4 + H2O ⇄ NH3 + H3O+
Niewielką objętość przygotowanego roztworu umieszczono w probówce, do której dodano kilka kropel błękitu bromotymolowego.
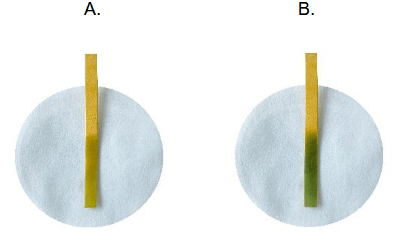
Oblicz pH otrzymanego roztworu. Wynik podaj w zaokrągleniu do jednego miejsca po przecinku. Następnie wybierz zdjęcie, na którym przedstawiono wygląd zawartości probówki po dodaniu do niej wskaźnika, i zaznacz literę A, B albo C.