Informator CKE, Poziom rozszerzony (Formuła 2023) - Zadanie 41. (2 pkt)
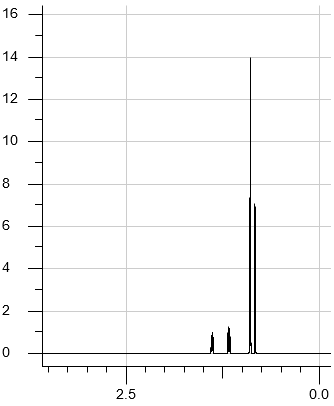
Jedną z najważniejszych metod fizykochemicznych stosowanych do badania struktury związków organicznych jest spektroskopia magnetycznego rezonansu jądrowego, NMR. Wykorzystuje się w niej właściwość polegającą na tym, że jądra atomów większości pierwiastków mają niezerowy spin. Najczęściej wykorzystuje się izotop wodoru 1H, którego jądra – czyli protony – są opisane liczbą spinową ½. Po umieszczeniu w silnym polu magnetycznym protony mogą się znajdować w dwóch stanach energetycznych – podstawowym i wzbudzonym. Aby wykonać pomiar, umieszcza się próbkę badanego związku w polu magnetycznym i wzbudza jądra 1H za pomocą fal radiowych. Powrót jąder ze stanu wzbudzonego do stanu podstawowego skutkuje wysłaniem sygnału rejestrowanego za pomocą detektora. Częstotliwość tego sygnału zależy od położenia atomów w cząsteczce. Zarejestrowane sygnały tworzą obraz zwany widmem NMR (rysunek poniżej), które dostarcza ważnych informacji o budowie cząsteczki związku.
Liczba sygnałów w widmie jest równa liczbie grup równocennych atomów wodoru w cząsteczce związku. Przykładowo – w cząsteczce octanu etylu obecne są trzy grupy równocennych atomów wodoru: dwie różne grupy –CH3 i jedna grupa –CH2–, czyli w widmie są obecne trzy sygnały. Te sygnały mogą mieć w określonych przypadkach złożony kształt, co w pokazanym widmie skutkuje ich rozszczepieniem (poszerzeniem).
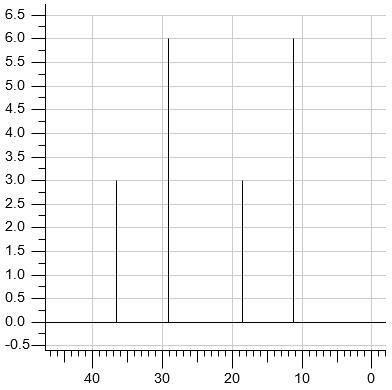
Drugim nuklidem często wykorzystywanym w pomiarach NMR jest izotop węgla 13C, którego zawartość w naturalnym węglu wynosi ok. 1%. Jego jądro ma także spin ½, w odróżnieniu od izotopu 12C, którego jądra mają spin zerowy i dlatego są nieaktywne w NMR. Widma NMR węgla 13C rejestruje się w taki sposób, że sygnały są pojedynczymi liniami.
W cząsteczce octanu etylu są cztery nierównocenne atomy węgla, w związku z czym w widmie 13C są obecne cztery sygnały.
Na podstawie analizy elementarnej ustalono wzór sumaryczny alkanu A: C5H12. Analiza widm NMR dla związku A dała następujące wyniki: w widmie 1H NMR znajduje się jeden sygnał, w widmie 13C NMR znajdują się dwa sygnały. Związek A i jego pochodne poddano przemianom, które ilustruje poniższy schemat:
A +Br2, UV A1 +NaOH, H2O A2 +CuO, T A3
Stwierdzono, że stosunek ilościowy atomów wchodzących w skład cząsteczki związku A3 wynosił NC : NH : NO = 5 : 10 : 1.
Podaj nazwę systematyczną związku A oraz wzór półstrukturalny (grupowy) związku A3 i uzupełnij tabelę: określ liczbę sygnałów w widmach 1H NMR i 13C NMR dla związku A3.
Nazwa systematyczna związku A:
Wzór półstrukturalny (grupowy) związku A3:
| Liczba sygnałów dla związku A3 | |
| w widmie 1H NMR | w widmie 13C NMR |