Matura Maj 2023, Poziom rozszerzony (Formuła 2023) - Zadanie 3. (1 pkt)
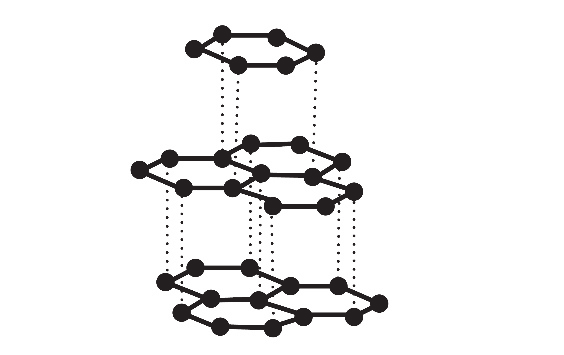
Węgiel tworzy kilka odmian alotropowych, które różnią się strukturą krystaliczną. Są wśród nich diament, grafit i fulereny.
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe.
| 1. | Odmienna budowa wewnętrzna diamentu, grafitu i fulerenów jest przyczyną różnic ich właściwości chemicznych, przy zachowaniu identycznych właściwości fizycznych. | P | F |
| 2. | W krysztale diamentu każdy z atomów węgla tworzy kowalencyjne wiązania 𝜎 z czterema otaczającymi go atomami. | P | F |