Matura Maj 2023, Poziom rozszerzony (Formuła 2023) - Zadanie 11. (4 pkt)
Krzywa wiązania tlenu przedstawia wysycenie cząstkowe hemoglobiny w zależności od ciśnienia cząstkowego tlenu. Wysyceniem cząstkowym nazywa się stosunek liczby miejsc zawierających związany tlen do całkowitej liczby miejsc zdolnych do wiązania tlenu w cząsteczkach hemoglobiny.
Na wiązanie tlenu przez hemoglobinę wpływają różne czynniki, m.in. stężenie 2,3-bisfosfoglicerynianu (2,3-BPG) w erytrocytach.
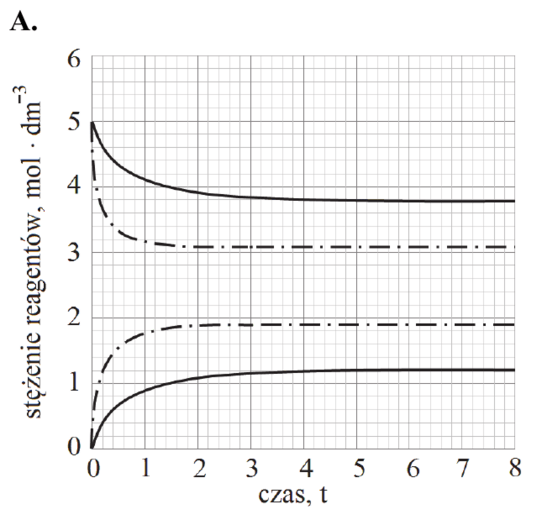
Na wykresie przedstawiono dwie krzywe wiązania tlenu:
- czarna krzywa przedstawia dane uzyskane z użyciem ludzkiej hemoglobiny oczyszczonej (wyizolowanej z erytrocytów)
- czerwona krzywa przedstawia dane uzyskane z użyciem ludzkiej hemoglobiny znajdującej się w erytrocytach.
Na osi X zaznaczono typowe wartości ciśnienia cząstkowego tlenu występujące w płucach oraz w tkankach innych narządów organizmu.
11.1. (0–2)
Oceń, czy poniższe stwierdzenia dotyczące wiązania tlenu przez hemoglobinę są prawdziwe. Zaznacz P, jeśli stwierdzenie jest prawdziwe, albo F – jeśli jest fałszywe.
| 1. | Oczyszczona hemoglobina ma większe powinowactwo do tlenu niż hemoglobina w erytrocytach. | P | F |
| 2. | Przy ciśnieniu cząstkowym tlenu równym 100 mmHg oczyszczona hemoglobina wiąże o 8% więcej tlenu niż hemoglobina w erytrocytach. | P | F |
| 3. | Maksymalne możliwe wysycenie cząstkowe hemoglobiny tlenem zależy od związania hemoglobiny z 2,3-BPG. | P | F |
11.2. (0–1)
Wiązanie 2,3-BPG z hemoglobiną płodową jest znacznie słabsze niż z hemoglobiną dorosłego człowieka. U ciężarnych kobiet stężenie 2,3-BPG w erytrocytach jest o 30% wyższe niż u kobiet niebędących w ciąży.
Uzupełnij poniższe zdanie tak, aby w poprawny sposób przedstawiało wpływ 2,3-BPG na wiązanie tlenu przez hemoglobinę. W każdym nawiasie podkreśl właściwe określenie.
Podwyższone stężenie 2,3-BPG w erytrocytach ciężarnych kobiet jest przyczyną (obniżonego / podwyższonego) powinowactwa hemoglobiny matki do tlenu, co (ułatwia / utrudnia) dyfuzję tlenu z części macicznej łożyska do części płodowej łożyska.
11.3. (0–1)
Podaj przykład funkcji pełnionej przez hemoglobinę w erytrocytach, innej niż transportowanie tlenu.