Informator CKE, Poziom rozszerzony (Formuła 2023) - Zadanie 43. (2 pkt)
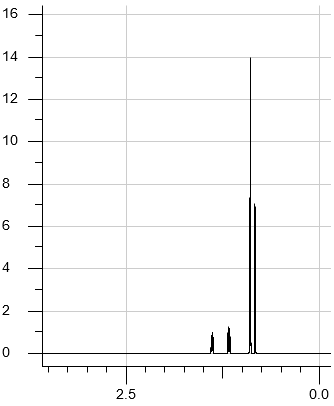
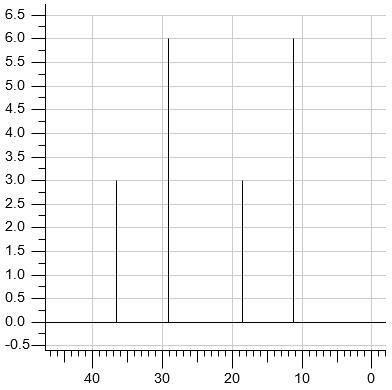
Dwa węglowodory aromatyczne – A i B – mają wzór sumaryczny C8H10. Izomer A w wyniku reakcji nitrowania tworzy wyłącznie jedną mononitropochodną. Izomer B poddany reakcji monochlorowania w obecności światła, a następnie – reakcji z wodnym roztworem KOH, tworzy alkohol drugorzędowy.
43.1. (0–1)
Napisz równanie reakcji mononitrowania związku A – zastosuj wzory półstrukturalne (grupowe) lub uproszczone związków organicznych. Podaj nazwę systematyczną produktu mononitrowania związku A.
Równanie reakcji:
Nazwa systematyczna produktu mononitrowania związku A:
43.2. (0–1)
Uzupełnij schemat ciągu przemian prowadzonych od związku B do alkoholu. Związki organiczne przedstaw za pomocą wzorów półstrukturalnych (grupowych) albo uproszczonych.